ฮีสทิดีน: สูตรปฏิกิริยาทางเคมี
เราแต่ละคนอย่างน้อยหนึ่งครั้งในชีวิตของฉันคิดถึงอาหารของมัน ตัวอย่างเช่นสิ่งที่อัตรารายวันของสารต่างๆที่จำเป็นสำหรับร่างกายมาให้เรากับอาหาร? กรดอะมิโนที่เราต้องการคืออะไร? วันนี้เราจะไม่พูดเกี่ยวกับโภชนาการที่เหมาะสมโดยรวมเนื่องจากไม่มีบทความเกี่ยวกับเรื่องนี้มากพอหรือแม้แต่บทความหนึ่งโหล เราจะบอกเพียงเรื่องเดียวเท่านั้นซึ่งเป็นสิ่งที่สำคัญมากสำหรับสิ่งมีชีวิต นี่คือกรดฮิวมิดีนในกรดอะมิโน ชื่อทางเคมีของมันฟังดูซับซ้อน - กรด L-2-amino-3- (1H-imidazol-4-yl) propanoic แต่เกี่ยวกับทุกอย่างตามลำดับ
กรดอะมิโนคืออะไร?
ก่อนที่จะอภิปรายคุณสมบัติของ histidine และของมันบทบาทในร่างกายเราจะเข้าใจแนวคิดเรื่อง "กรดอะมิโน" ผู้ที่ชอบกีฬาได้ยินเกี่ยวกับสารเหล่านี้ กรดอะมิโนเป็นสารประกอบอินทรีย์ที่มีสองกลุ่มฟังก์ชันพื้นฐานที่ทำให้เป็นพิเศษ: กลุ่มอะมิโน - NH2 และกลุ่มคาร์บอกซิลที่เรียกว่า -COOH
ประการแรกต้องรับผิดชอบต่อคุณสมบัติพื้นฐานของเรื่องนี้คลาสผิดปกติของสาร ไนโตรเจนและคู่อิเล็กตรอนของมันทำให้กรดอะมิโนสามารถสร้างประจุบวกได้ ในกรณีนี้กลุ่มอะมิโนจะเปลี่ยนเป็นไอออนดังกล่าว: -NH3+.

กลุ่มที่สองทำงานเป็นผู้รับผิดชอบต่อคุณสมบัติของกรด มีความสามารถในการให้โปรตอนเปลี่ยนเป็นแอนติเจน COO-. ปรากฏการณ์นี้ทำให้สามารถสร้างเกลือจากกลุ่มคาร์บอกซิลได้
ดังนั้นกรดอะมิโนมีสองส่วนซึ่งแต่ละชนิดมีความสามารถในการสร้างเกลือได้ หนึ่งในนั้นให้สารเหล่านี้ที่มีคุณสมบัติเป็นกรดและอีกส่วนหนึ่งเป็นเบส โดยทั่วไปกรดอะมิโนสามารถแสดงได้ดังนี้ NH2-CH (R) -COOH ตัวอักษร R จะเข้าใจนี่เป็น "รุนแรง" นั่นคืออนุภาคใด ๆ อินทรีย์ประกอบด้วยการทำงานเป็นกลุ่มและโครงกระดูกคาร์บอนและความสามารถในการสร้างพันธะ (หรือพันธบัตร) กับสารตั้งต้นโมเลกุลกรดอะมิโน
ตามกฎแม้แต่ผู้ที่ไม่คุ้นเคยกับเภสัชวิทยาและไม่ได้มีส่วนร่วมในกีฬาอย่างน้อยได้ยินครั้งหนึ่งแม้จากการโฆษณาที่เราต้องกรดอะมิโนและมีประโยชน์มาก ลองคิดดูว่าหน้าที่ของพวกเขาทำอะไรในร่างกายและทำไมคุณต้องได้รับในอัตราที่จำเป็นจากอาหาร
หน้าที่ของกรดอะมิโนในร่างกาย
ดังที่คุณทราบเราประกอบด้วยโปรตีนไขมันและคาร์โบไฮเดรต และเรากินอาหารเพื่อรักษาชีวิตของเราไว้ แต่ในเรื่องของบทความนี้เราสนใจเฉพาะโปรตีนเท่านั้น เหล่านี้เป็นโมเลกุลขนาดใหญ่ที่ทำหน้าที่แตกต่างกันอย่างสิ้นเชิงและสำคัญมากในร่างกายของเรา: การขนส่งสารการสร้างเซลล์ใหม่เสริมสร้างความเข้มแข็งของการเชื่อมต่อระหว่างเซลล์ประสาทของสมอง
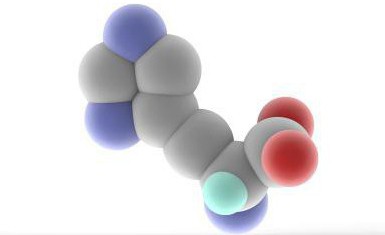
ฮิสติดีน
สูตรของกรดอะมิโนใด ๆ รวมถึงตามที่เรามีอยู่แล้วได้พบอย่างน้อยสองกลุ่มการทำงานและโครงกระดูกคาร์บอนเชื่อมต่อพวกเขา นั่นคือเหตุผลที่ความแตกต่างระหว่างกรดอะมิโนทั้งหมด (ซึ่งโดยวิธีการนี้พบได้หลายล้านตัวแล้ว) คือความยาวของสะพานคาร์บอนระหว่างสองกลุ่มและโครงสร้างของอนุมูลอิสระที่ยึดติดกับมัน

หัวข้อของบทความของเราเป็นหนึ่งในกรดอะมิโน -ฮิสติดีน สูตรของกรดที่ไม่อาจถูกแทนที่นี้ไม่ใช่เรื่องง่าย ในห่วงโซ่คาร์บอนหลักระหว่างสองกลุ่มหน้าที่เราจะเห็นเพียงหนึ่งอะตอมคาร์บอน ในความเป็นจริงกรดอะมิโนกรดโปรตีนที่จำเป็น (สามารถสร้างกรดอะมิโนโปรตีน) ยังมีอะตอมของคาร์บอนเพียงตัวเดียวในห่วงโซ่นี้ นอกจากนี้ histidine มีโครงสร้างอนุมูลอิสระที่ซับซ้อนประกอบด้วยวัฎจักร ด้านบนคุณสามารถดูสิ่งที่เป็น histidine สูตรที่มีลักษณะโครงสร้างเป็น heterocycle (รวมอะตอมอื่น ๆ ที่ไม่ใช่คาร์บอน) ไม่ได้เป็นสารที่ซับซ้อนมากนัก
ดังนั้นเมื่อเราได้วิเคราะห์แนวคิดพื้นฐานแล้วเราจึงหันมาทำปฏิกิริยาที่สามารถทำกับ histidine ได้
สมบัติทางเคมี
ปฏิกิริยาที่กรดอะมิโนตัวนี้เข้าสู่,น้อยมาก นอกเหนือไปจากการเกิดปฏิกิริยากับกรดและเบสแล้วจะเกิดปฏิกิริยา biuret ขึ้นรูปผลิตภัณฑ์สี นอกจากนี้ histidine ซึ่งเป็นสูตรที่มีสารตกค้างของ imidazole สามารถทำปฏิกิริยากับกรด sulfanilic ในปฏิกิริยา Pauli ได้

ข้อสรุป
บางทีเราได้ถอดประกอบรายละเอียดหลักทั้งหมด เราหวังว่าบทความนี้จะเป็นประโยชน์สำหรับคุณและให้ความรู้ใหม่แก่คุณ
</ p>


